
miércoles, 17 de junio de 2015
EFECTO VENTURI (DAVID)
> Pulverizador casero: para realizar esto necesitaremos una pajita y un vaso de agua. En primer lugar cortaremos la pajita por la zona que se hunde para llevarnos aproximadamente 1/3 de la pajita. Abriremos esta parte verticalmente con unas tijeras y la enrollaremos sobre sí misma. Acontinuacion haremos un agujero lo suficientemente ancho para que entre el trozo enrollado a la altura de la mitad de la pajita. Por último introduciremos este artilugio en un vaso de agua de tal manera que la zona enrollada toque el agua y las demás no, y veremos como al soplar (aumentamos la velocidad) baja la presión dentro de la pajita y esto hace que suba el agua por la zona enrollada y salga por el extremo opuesto al que se sopla


domingo, 14 de junio de 2015
LEY DE HOOKE JAVI(FOTOS) Y DAVID(EXPLICACION)
 Una de las pesas que vamos a utilizar para comprobar cuanto se estira el muelle dependiendo del peso que ejrzamos en él.
Una de las pesas que vamos a utilizar para comprobar cuanto se estira el muelle dependiendo del peso que ejrzamos en él. La medicion del muelle sin que este esté estirado.
La medicion del muelle sin que este esté estirado. La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos.
La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos. La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos.
La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos. Una de las pesas que vamos a utilizar para comprobar cuanto se estira el muelle dependiendo del peso que ejrzamos en él.
Una de las pesas que vamos a utilizar para comprobar cuanto se estira el muelle dependiendo del peso que ejrzamos en él. La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos.
La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos. La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos.
La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos. La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos.
La medición de la longitud del muelle cuando hemos echo que se estire gracias a el peso que hemos ejercido. Esta nos valdrá para diferenciar de la longitud de otros pesos.
EN ESTA FOTO PODEMOS VER LO QUE MIDE DE ANCHO EL MUELLE QUE VAMOS A UTILIZAR ESTO LO HACEMOS PARA AL ALARGARSE EL MUELLE RESTAR EL ALAGAMIENTO TOTAL DEL ANCHO DEL MUELLE PARA OBTENER EL ALARGAMIENTO EXACTO QUE PRODUCE CADA PESA.
EN ESTA FOTO OBSERVAMOS LA PESA CON SU MASA CORRESPONDIENTE
LA LEY DE HOOKE LE HEMOS EXPLICADO MEDIANTE EL ALARGAMIENTO DE UN MUELLE CON RESPECTO A PESAS DE DIFERENTES MASAS
miércoles, 10 de junio de 2015
PRENSA HIDRAULICA (JAVI)
PRENSA HIDRAULICA.
- Comproeba que la presión en el interior de un líquido es perpendicular a las paredes.
- El Principio de Pascal, el cual dice, que "la presión ejercida sobre un líquido se transmite por igual a cada punto del líquido y en todas las direcciones"
- Demostrar que con una fuerza pequeña se puede mover un peso grande.
TENSIÓN SUPERFICIAL ( NACHO)
El concepto de tensión superficial se emplea en el ámbito de la física para hacer referencia a la cantidad de energía que se requiere para incrementar la superficie de un líquido por unidad de área. Dicha energía se necesita ya que los líquidos ejercen una resistencia a la hora de incrementar la superficie.
MATERIALES:
- Pelota de ping pong
- Cristalizador
- Lo primero es dejar una pelota de ping pong en un cristalizador medio lleno de agua, al dejar la pelota podemos observar que la pelota es atraída por el cristal y va hacia él
- Lo segundo es dejar otra pelota de ping pong en otro cristalizador lleno de agua hasta el borde, y aquí podemos observar que la pelota no es atraída por el cristal y se queda en e l centro del creistalizador
lunes, 8 de junio de 2015
PRESIÓN EN UN GLOBO ( NACHO)
MATERIALES:
- Tubo de ensayo
- Globo
- Mechero
- Agua
- Barra de soporte
- Se mete agua en una probeta
- Se pone un globo en la boquilla de la probeta
- Se enciende el mechero debajo de la probeta haciendo que la presión del calor haga que el globo se infle
DIFERENCIA DE PRESIÓN( NACHO, DAVID Y JAVI) SUBIDO POR NACHO
MATERIALES.
- Lata
- Agua
- Pinzas
- Mechero
- Primero ponemos un poco de agua en una lata
- Después se calienta la lata con un mechero
- Cuando se caliente se hecha la lata al bol de agua de dos maneras diferentes, una despacio donde la lata se comprime poco y otra deprisa donde la lata se comprime mucho
en clase
domingo, 7 de junio de 2015
EXPULSIÓN DE CO2 (NACHO , JAVI,DAVID) SUBIDO POR NACHO
MATERIALES:
- Una barra de soporte
- Un tubo de ensayo (con tapón)
- Un poco de agua
- Mechero
- Llenar una probeta con un poco de agua
- Poner la probeta de la barra de soporte con un poco de inclinación
- encender el mechero justo debajo de la probeta y esperar a que salga el tapón debido a la presión que ejerce el fuego
jueves, 23 de abril de 2015
Saponificación ( NACHO)
Lo primero que hemos hecho ha sido coger 4 gramos de sosa cáustica


Lo segundo que hemos hecho ha sido coger 20mL de aceite y después otros 20mL de agua


el siguiente paso fue mezclar todas las cosas ya pesadas o medidas( la sosa, el aceite y el agua) en un vaso de plástico
Y ya mezclado todo, se dejan unos días para que se solidifique hasta que nos salga una muestra de jabón
martes, 21 de abril de 2015
Neutralizacion (David)
NEUTRALIZACION
Así comprobamos que el vinagre es el ácido.Así comprobamos que el amoniaco es la base.
Así queda una vez neutralizado el ácido y la base
Almidón. (Javi y David)
DESPUÉS.
ANTES.
La práctica consistía en mezclar una pequeña cantidad de agua con almidón y echar lugol sobre ella. De esa manera la mezcla se queda de color negro.
A continuación se calienta levemente con un mechero de alcohol de manera que se neutraliza y se quedara transparente la mezcla.
ANTES.
REACCIÓN QUÍMICA DEL ALMIDÓN.
La práctica consistía en mezclar una pequeña cantidad de agua con almidón y echar lugol sobre ella. De esa manera la mezcla se queda de color negro.
A continuación se calienta levemente con un mechero de alcohol de manera que se neutraliza y se quedara transparente la mezcla.
Nitrato de plata (AgNO3) (Javi)
NITRATO DE PLATA.
Esta reacción quimica consisitia en mezclar agua (H2O) con nitrato de plata en una probeta de manera que al vertir ambos fluidos estos quedaran con un color blanco, hay que contar con que ambas sustancias son transparentes. Estos son los pasos que he hecho:
- Hechas la disolución salina en la probeta, la llenas unos 15ml.
- Despúes de esto la viertes en un tubo de ensayo
- El siguiente paso es vertir el nitrato de plata en el agua con un cuentagotas, de manera que al principio queda una gruesa capa blanca en la parte de arriba de la botella.
- El último paso es con una barilla remover el recipiente hasta que ambos fluidos adquieran el se unan y adquieran un color blanco

MATERIALES:
- Una probeta.
- Un tubo de ensayo.
- Una barra de soporte.
- Un cuentagotas
- Nitrato de plata.
- La concentración salina.
Luvia de oro (Javi)
`` LLuvia de oro´´
Para realizar esta reacción realizaremos los siguientes pasos:
- Ponemos el tubo de ensayo en una barra de soporte, esta debe estar bien fijada para que no se caiga el tubo.
- A continuación vertemos el nitrato de plomo (Pb (NO3) (nosotros llenamos el tubo de ensayo un poco más de la mitad) en el tubo de ensayo, tras esto echaremos el yoduro potásico (KI) sobre el nitrato de plomo.
- Al contactar ambas sustancias aparecce un fluido amarillo en el nitrato de plomo, ha esto se le denomina "lluvia de oro"
- Una barra de soporte.
- Un tubo de ensayo.
- Nitrato de plomo (Pb (NO3)2).
- Agua.
martes, 7 de abril de 2015
NEUTRALIZACIÓN ( NACHO).
NEUTRALIZACIÓN.
Lo primero que hay que hacer en esta reacción es coger la fenolftaleína y el anaranjado de metilo, y después de eso cogemos dos ácidos H2SO4 y NAOH( ácido base)
Después de obtener esos productos tenemos que mezclar cada uno de los ácidos con la fenolftaleína y con el anaranjado de metilo.
Y lo último que hay que hacer es mezclar 20 ml de NAOH con la fenolftaleína y esto nos debería de quedar un color rosado y después con un cuentagotas ponemos H2SO4 haciendo que se neutralize y se quede transparente.

INTRODUCCIÓN. (Javi)
PBL REACCIONES QUÍMICAS.
Este PBL trata de realizar diferentes reacciones químicas, estas consisten en producir una serie de cambios físicos y químicos en los productos usados, cada reacción consta de unos reactivos y uno o varios productos.
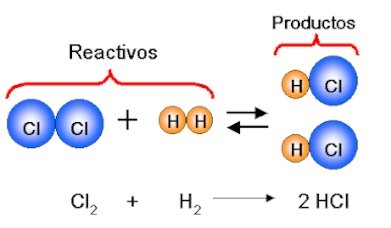 Este es el estilo que todas las reacciones químicas siguen.
Este es el estilo que todas las reacciones químicas siguen.
 Este es el estilo que todas las reacciones químicas siguen.
Este es el estilo que todas las reacciones químicas siguen.
En este PBL realizaremos varias reacciones químicas, además de una propia de cada grupo; las reacciones qúímicas que vamos a realizar son:
- Neutralización e indicador ácido-base.
- Saponificación.
- Precipitación.
- Presencia de almidón a través de una disolución de yodo y la variación de la temperatura.
- La reacción propia de cada grupo.
sábado, 21 de marzo de 2015
Punto 1 y punto 5. (Nacho)
- En esta imagen se pueden ver los calculos y el proceso del punto 1 y el punto 5.
En el punto uno teniamos que hayar la densidad de la disolución, para ello hemos usado la fórmula de la densidad:
Densidad = masa/volumen.
Punto 2.
En este punto teníamos que hayar el volumen que se le tendría que dar al viajero que contuviera los 12 gramos de sal. Para ello hemos usado la fórmula de la densidad:
Densidad = masa/volumen.
viernes, 20 de marzo de 2015
Punto 2 y 4 concentracion y beneficio del viajero(David)
PROCESO:
Punto 2
1.Lo primero que he hecho a sido hallar los gramos de soluto que eran necesarios para hallar la concentración.
2.Después he hallado la concentración.
Punto 4
1.Me he enterado de los datos que se daban, es decir , de lo q costaba cada gramo de sal según el problema.
2.He hallado mediante una regla de tres lo que se llevaria el viajero por los 50cc d esa disolución de sal
Punto 3 PBL disoluciones. (Javi)
 Proceso.
Proceso. Peso del cristalizador con la sal.
Peso del cristalizador con la sal. Peso del cristalizador.
Peso del cristalizador.- En este punto hemos tenido que confeccionar una etiqueta en la que hemos calculado la concentración que había en nuestra disloución y los moles/litro.
- Para esto hemos necesitado saber cuanto era el peso del soluto, lo hemos calculado cogiendo el peso del cristalizador con la sal y restándoselo del cristalizador.
- Hemos usado factores de conversión para cambiar los ml a l.
- FÓRMULAS
Concentración= g soluto/l disolución.
Molaridad= nºde moles del soluto/l disolución.
martes, 10 de marzo de 2015
INTRODUCCIÓN
INTRODUCCIÓN DE DISOLUCIONES
Desde tiempos remotos se comercializaba con sal. Llegó a ser tan valiosa que por cada gramo se pagaba 1000$.
Un día se presentó en el almacén un viajero llevando un frasco en el que había disuelto sal.
Desconocía la concentración de la mezcla, pero este pretendía:
- Que le pagaran, a 1000$/gramo, la sal que estuviera en 50 cc de disolución.
- Además se llevaría el volumen de disolución que contuviera 23 gramos de sal y el resto lo donaría a cambio de etiquetar el frasco con su concentración en g/l, en molaridad y con su densidad.
- Para resolver este problema llamó ha científicos y les ofreció el 10% del beneficio de la venta a cambio de realizar por él todos los cálculos necesarios.

martes, 10 de febrero de 2015
DECANTACIÓN
DECANTACIÓN
Decantación.
- Lo primero que hemos hecho ha sido coger dos buretas.
- Después hemos llenado uno de 20 cc de agua y el otro de 20 cc de aceite.
- Después de esto hemos juntado ambas en un matraz de destilación.
- Poco a poco hemos abierto la llave que tiene el matraz hasta dejar que caiga el agua que se habia quedado en el fondo ya que este tiene mayor densidad que el aceite.
- Cuando ha caido la primera gota de aceite se cierra la llave y compruebas que la cantidad final sea igual a la inicial.
Suscribirse a:
Entradas (Atom)


































